| 碘化钐 基本信息 | |||
|---|---|---|---|
| CAS号 | 32248-43-4 | 分子式 | I2Sm |
| 分子量 | 404.16920 | 精确质量 | 405.72870 |
| PSA | 0.00000 | LogP | 1.77140 |
 基本信息
展开↓
基本信息
展开↓  生产制备方法及用途展开↓
生产制备方法及用途展开↓按照标准的实验步骤从金属钐和碘在THF中来制备[1]。
碘化钐(SmI2)是有机合成中一个具有广泛用途的试剂。它参与的主要反应包括:自由基环化反应;羰基-烯烃偶联反应;频哪偶联反应;羟醛缩合反应;Barbier反应;Reformatsky反应等。已经有多篇论文对它们的性质和应用进行了详细的综述[2]。
SmI2最基本的反应是它的还原反应。在HMPA作为共溶剂的情况下,它可以方便地除去底物分子中的卤原子 (式1)[3]。在可见光照射的情况下,不使用HMPA 也可以得到同样的结果[4]。杂原子键,例如N-N[5]或者N-O[6]键,在SmI2的作用下能够发生选择性断裂,这种性质在多官能团复杂化合物的合成中特别有用 (式2)。
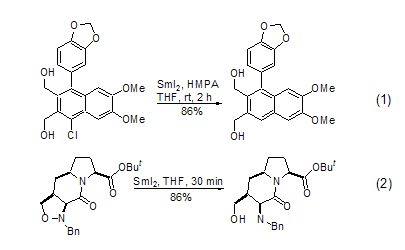
SmI2的特征反应之一是在一分子醛的存在下,1,3-羟基酮在低温下数分钟内被还原成为1,3-二羟基化合物的单酯衍生物。反应的机理可能是通过一个环状过渡态进行的,所以反应中新形成的羟基保持高度的立体选择性 (式3)[7,8]。α-羟基酮在SmI2的作用下,一分钟之内可以将羟基除去生成相应的酮 (式4)[9~11]。
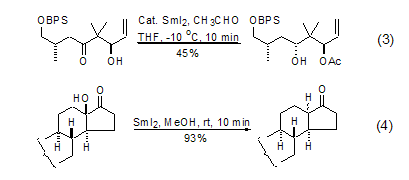
二醛在SmI2的作用下发生频呐醇偶联反应,生成大环化合物。该反应不仅反应条件简单,而且给出比较满意的产率 (式5)[12,13]。SmI2参与的最有价值的反应是羰基-烯烃偶联反应。使用带有拉电子基团的缺电子烯烃有助于提高反应的收率 (式6)[14,15]。
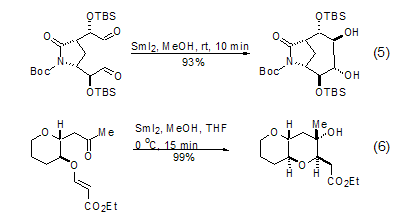
 物化性质展开↓
物化性质展开↓
贮存:一般保存于约0.1mol/L的四氢呋喃溶液中。
1.如果遵照规格使用和储存则不会分解,未有已知危险反应。
2.遇水分解生成碱式碘化钐和氢气。有强还原性。
3.具有较强的吸湿性,对氧气特别敏感,需要在惰性气体保护下制备和使用。
1.性状:蓝色-深蓝色液体,具有特殊气味。
2.密度(g/mL,25℃):0.922
3.相对蒸汽密度(g/mL,空气=1):未确定
4.熔点(ºC):527
5.沸点(ºC,常压):1580
6.沸点(ºC,KPa):未确定
7.折射率:未确定
8.闪点(ºC):-18.9
9.比旋光度(º):未确定
10.自燃点或引燃温度(ºC):未确定
11.蒸气压(Pa,20ºC):未确定
12.饱和蒸气压(KPa,25ºC):未确定
13.燃烧热(KJ/mol):未确定
14.临界温度(ºC):未确定
15.临界压力(KPa):未确定
16.油水(辛醇/水)分配系数的对数值:未确定
17.爆炸上限(%,V/V):未确定
18.爆炸下限(%,V/V):未确定
19.溶解性:在极性有机溶剂中有一定的溶解度,通常在THF,HMPA中使用。
 安全信息展开↓
安全信息展开↓  毒理性展开↓
毒理性展开↓
急性毒性:
Oral:LD50:2300mg/kg(gpg)
LD50:1650mg/kg(rat)
Inhalative:LC50/3H:21000ppm/3H(rat)
主要的刺激性影响:
在皮肤上面:刺激皮肤和粘膜。
在眼睛上面:刺激的影响
致敏作用:没有已知的敏化作用。
总括注解
水危害级别1(德国规例)(通过名单进行自我评估)该物质对水有稍微危害的。
不要让未稀释或大量的产品接触地下水、水道或污水系统。
若无政府许可,勿将材料排入周围环境。
 MSDS 展开↓
MSDS 展开↓ 分子结构与计算化学数据展开↓
分子结构与计算化学数据展开↓
1、 疏水参数计算参考值(XlogP):
2、 氢键供体数量:0
3、 氢键受体数量:0
4、 可旋转化学键数量:0
5、 互变异构体数量:
6、 拓扑分子极性表面积(TPSA):0
7、 重原子数量:3
8、 表面电荷:0
9、 复杂度:2.8
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1